خلايا الميثانول Direct Methanol Fuel Cells :
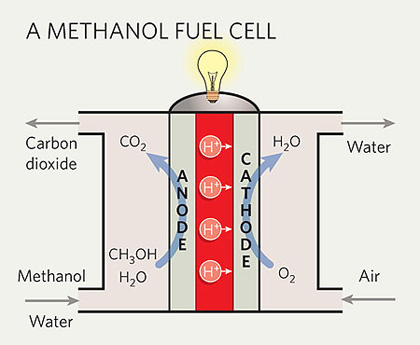
التقنية المستخدمة في خلايا الميثانول (DMFC) لازالت بمراحل مبكرة من التطور، لكنها مرشحة للاستخدام بتغذية الهواتف النقالة والكمبيوترات المحمولة بالسنوات المقبلة. خلايا الميثانول مشابهة لخلايا الوقود ذات غشاء التبادل الالكتروني بأن لها وسيط بولميري وحاملات الشحنة هي ايونات الهيدروجين (البروتونات)، لكن الميثانول السائل (CH3OH) يؤكسد بوجود الماء في القطب الموجب ويولد ثاني أكسيد الكربون CO2, وايونات الهيدروجين والالكترونات التي تسري بالدارة الخارجية مكونة تيار كهربائي. ايونات الهيدروجين تعبر من خلال الوسيط وتتفاعل مع الأكسجين من الجو ومع الالكترونات من الدارة الخارجية وتشكل ماء عند القطب السالب .
|
Anode Reaction: |
CH3OH + H2O ⇒ CO2 + 6H+ + 6e– |
|
Cathode Reaction: |
3/2 O2 + 6 H+ + 6e– ⇒ 3 H2O |
|
Overall Cell Reaction: |
CH3OH + 3/2 O2 ⇒ CO2 + 2 H2O |
طورت هذه الخلايا في أوائل التسعينات لكنها لم تستخدم بسبب كفاءتها وكثافة الكهرباء المنخفضة لها وبعض المشاكل الأخرى. بعض التحسينات التي أجريت على المحفزات والتطورات الأخرى زادت الكثافة الكهربائية 20 ضعف وبالنسبة للمردود قد يصل في النهاية إلى 40 %. اختبرت هذه الخلايا بدرجات حرارة ما بين 50ºC-120ºC .درجة الحرارة المنخفضة هذه وعدم الحاجة لمولد وقود جعلت من خلايا الميثانول مرشح جيد للتطبيقات الصغيرة والمتوسطة الحجم , مثل الهواتف الخلوية و الحواسيب المحمولة, إضافة إلى وسائل النقل. أحد العوائق لتقنية الميثانول هي إن عملية الأكسدة بدرجة الحرارة المنخفضة للميثانول ليتحول إلى ايونات الهيدروجين وأكسيد الكربون تحتاج إلى محفز أكثر نشاطاً, والذي يعني أننا نحتاج إلى المزيد من محفز البلاتينيوم غالي السعر مقارنة بخلايا الوقود ذات الغشاء البرتوني. هذه الكلفة الزائدة على أية حال يمكن أن تقابل الاقتصادية في هذا النظام بما إنه يعمل بدون الحاجة لنظام تشكيل الوقود وإمكانية استخدام وقود سائل. سبب أخر لتأخر تطوير هذا النوع من خلايا الوقود الكحولية هو أن الميثانول مادة سامة , لذا تقوم بعض الشركات بتطوير خلية وقود ايثانول Direct Ethanol Fuel Cell (DEFC) أداء خلايا الوقود هذه هو حاليا نصف ما تقدمه خلايا وقود الميثانول لكن هذا الأمر في قيد التطوير ويتوقع أن تصغر الفجوة بين أداء الخليتين بالمستقبل .

